
elektron - Negatív töltésű részecske: -1. A tömege kb. 1840-szor kisebb, mint a neutroné és a protoné.
proton - Pozitív töltésű részecske: +1. Az elektron tömegének 1840-szerese.
neutron - Tömege majdnem ugyanannyi, mint a protoné. Elektromos töltöttség szempontjából semleges: 0.
Az elektronok az atommagtól nagy távolságban keringenek, különböző elektronpályákon. Az elektronpályák számozása s, p, d, f. A jelzések az elektron térbeli és időbeli elosztását jelzik. (s - gömb felszín, p - "súlyzó" - egy síkkal, d - két sík által szabdalt szabályos, f - 3 sík által felosztott ). Az elektronpályák ebben a sorrendben egyre magasabb energiaszintről indulnak.
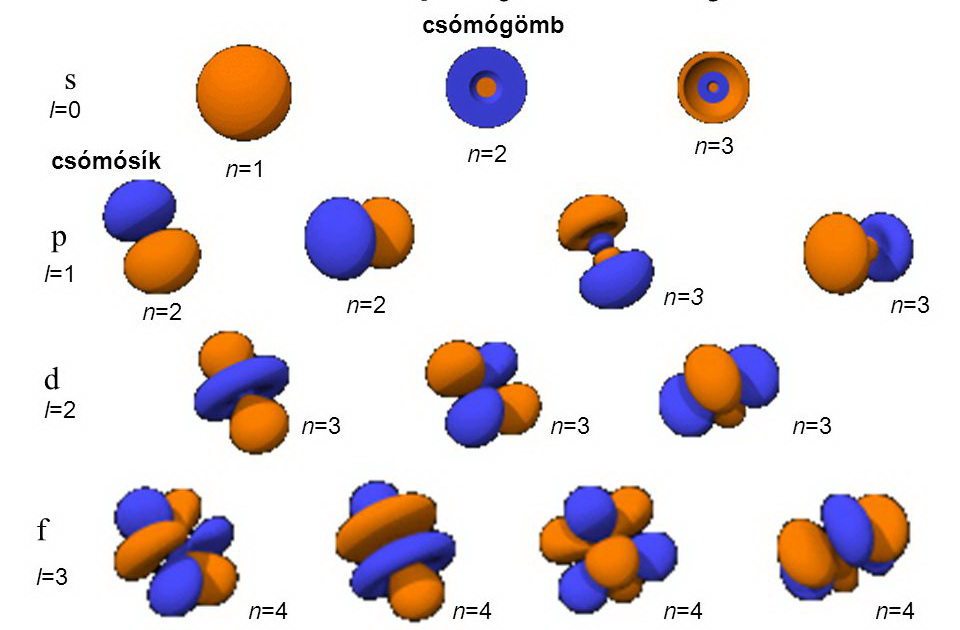
Az elektronok előfordulási valószínűsége a képzeletbeli síkok mentén a legkisebb. A rajzon ábrázolt gömb és egyéb felületek közelében a legnagyobb a valószínűség.
Az elektronok valahol mindig vannak, de a helyüket és a sebességüket együtt a Heisenberg-féle határozatlansági reláció miatt nem lehet pontosan egy időben meghatározni, ezért csak azt tudjuk mondani, hogy az elektron "nagyrészt" itt vagy ott tartózkodik.
Az atommagban lévő protonok és a körülötte keringő elektronok egymást vonzzák egymást, ugyanakkor minél kisebb helyre akarunk "beszorítani" egy elektront, annál nagyobb valószínűséggel szökik meg onnan és a két egymással ellentétes hatás hozza létre ezeket a furcsa felszíneket. Általában minden magára hagyott fizikai rendszer törekedik a legalacsonyabb energiaszintű állapot felé. Ez azt jelenti, hogy egy atomban az elektronok először mindig a legalacsonyabb energiaszintű állapotokat töltik be (S állapot), majd a P, D, és F állapotot, mert az energiaszintek így növekednek.
Az elektronok (a protonok és neutronok is ) pörögnek a tengelyük körül. Ezt a perdületet spin-nek hívják. A spin kétféle lehet. Ennek hatására az elektron (proton és neutron is) kissé eltérő energiaszinten van, ilyen módon egy elektronpályán két különböző spinű elektron lehetséges. A valós anyagban az elektronok olyan nagy számban vannak jelen, hogy bármilyen kémiai vagy egyéb fizikai hatás esetén a szabad helyekre mindig beugranak megfelelő spinű elektronok, ha az anyag szempontjából az alacsonyabb energiaszintet eredményez.